Le virus varicelle-zona (appelé VZV, pour varicella-zoster virus) est un herpès-virus persistant, également appelé HHV-3 (human herpes virus 3) ou herpès virus humain type 3, responsable chez l’être humain de la varicelle et du zona (herpes zoster).
Un virus persistant est un virus qui reste dans l’organisme à long terme, parfois à vie, sans forcément provoquer de symptômes constants. Il peut :
- Rester latent (inactif) puis se réactiver.
- Se multiplier à bas bruit, échappant au système immunitaire.
Le VZV ne doit pas être confondu avec d’autres herpès qui appartiennent cependant à la même famille comme
- Herpès labial dû à herpes simplex virus 1 ou HSV1. Il est responsable du bouton de fièvre. Sa réactivation peut être très fréquente, parfois plusieurs fois par an.
- L’herpès Génital dû à herpes simplex virus 2 ou HSV2
Le zona et la varicelle sont donc provoqués par le même virus, le virus varicelle-zona (VZV).
La varicelle représente la primo-infection, souvent contractée pendant l’enfance et considérée comme une maladie infantile bénigne. La varicelle se caractérise par une éruption cutanée avec des démangeaisons, de la fièvre et de la fatigue. La plupart des personnes contractent la varicelle pendant l’enfance et développent une immunité naturelle efficace et protectrice.
Le zona est une réactivation du virus VZV, survenant plus tard dans la vie car le VZV peut rester dans les ganglions rachidiens sous forme inactive malgré la guérison de la varicelle. Cette réactivation intervient souvent chez les personnes dont le système immunitaire est affaibli mais d’autres facteurs plus ou moins clairs interviennent. La réactivation du VZV se fait depuis un ganglion rachidien et provoque une éruption cutanée localisée au dermatome innervé par le ganglion rachidien. L’éruption est donc unilatérale, c’est-à-dire sur un seul côté du corps. L’éruption cutanée peut être très douloureuse et c’est le symptôme le plus gênant mis en avant par les patients qui cherchent donc à s’en protéger.
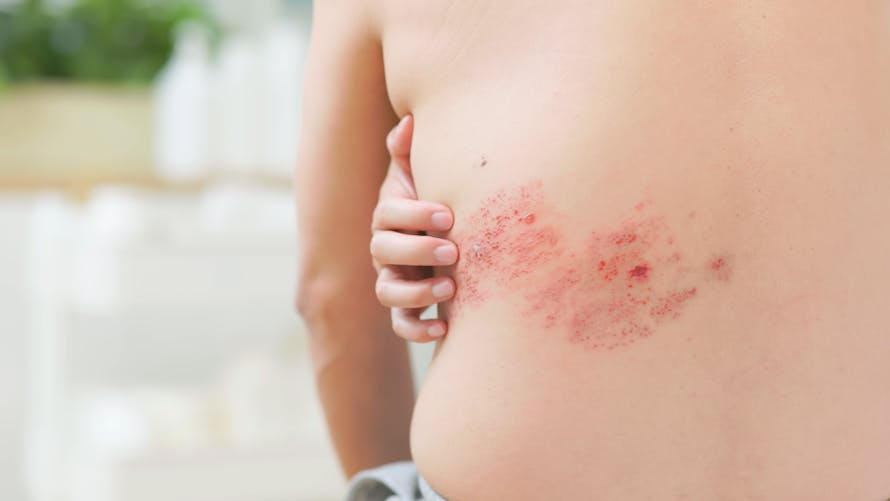
https://www.santemagazine.fr/sante/fiche-maladie/zona-177347and feel pain
Le vaccin Shingrix
Shingrix est un vaccin recombinant de la glycoprotéine E avec adjuvant (AS01B), destiné à la prévention du zona et des névralgies post-zostériennes chez les adultes de 50 ans et plus, ainsi que chez les adultes de 18 ans et plus présentant un risque accru de zona. Il est administré en deux doses, espacées de deux mois. Depuis le 14 décembre 2024, il est remboursé à 65% par l’Assurance Maladie pour les personnes concernées par les recommandations de la HAS [4]:
- chez les adultes de 65 ans et plus
- chez les adultes de 18 ans et plus présentant une immunodépression particulière
La demande de vaccination contre le zona est suffisamment importante pour que le vaccin Shingrix connaisse en 2025 des tensions d’approvisionnement. Il est contingenté en ville. [0]
Mais que disent les essais cliniques ?
Essai clinique du vaccin Shingrix
Un essai clinique a été publié en 2016 sous le titre :« Efficacité du vaccin Shingrix contre l’herpès-zona chez les adultes âgés de 70 ans ou plus » [1]
Les auteurs expliquent que la vaccination est une option intéressante pour réduire la charge de morbidité due à l’herpès-zona et à ses complications chez les personnes âgées.
Les auteurs (dont des employés du fabricant GSK) s’expliquent pourtant mal les raisons théoriques de l’efficacité de ce vaccin. Comment expliquer qu’en injectant un antigène de ce même virus et donc en restimulant le système immunitaire on puisse empêcher la réactivation du virus latent ?
Leur thèse est que l’inoculation d’un antigène viral (la glycoprotéine E contenue dans le vaccin) va restimuler l’immunité cellulaire, en particulier les lymphocytes T CD4+.
Les cellules T, en particulier les lymphocytes T CD4+ et CD8+, seraient essentielles pour maintenir cette latence en surveillant et en supprimant toute tentative de réactivation du virus. Ces lymphocytes T8 reconnaissent les antigènes viraux présentés par les cellules infectées et limiteraient la réplication virale. Cette explication de l’éventuelle efficacité du vaccin n’est pas pourtant prouvée.
Comment a été évaluée l’efficacité ?
Avant de commencer, il faut préciser que l’étude n’a pas intégré de patients ayant déjà eu un épisode de Zona. De même, les personnes immunodéprimées, qui sont parmi les plus susceptibles de subir des Zonas, ont aussi été exclues.
Ce choix est discutable car ces groupes semblent les plus légitimes à demander une vaccination efficace contre le Zona.
Il s’agit d’évaluer la protection contre les cas de zona.
Un cas suspect de zona est défini comme une éruption cutanée unilatérale accompagnée de douleur à l’exclusion de tout diagnostic alternatif. Si un cas n’est pas suspecté d’être un zona par l’investigateur, son évolution n’est pas suivie et il disparaît des statistiques (p46 protocole). Chaque cas suspect est identifié comme cas de zona si la PCR est positive ou bien si les cliniciens du comité de certification des cas votent en majorité pour un cas confirmé.
L’efficacité est aussi mesurée contre les douleurs post-zostériennes définies comme des douleurs sévères apparaissant ou s’aggravant plus de 90 jours après une éruption de zona.
Malheureusement de nombreuses modifications du protocole concernant les tests PCR et la définition des cas ne peuvent exclure que certains cas positifs chez les vaccinés et négatifs chez les placebo aient peut-être été requalifiés au cours de l’essai. [8]
Mais il y a plus grave. Le vaccin et le placebo n’avaient pas le même aspect. Malgré ce que les chercheurs affirment dans l’étude :
« The investigators, participants, and persons responsible for evaluating the study end points were unaware of whether HZ/su or placebo had been administered. »
« Les chercheurs, les participants et les personnes chargées d’évaluer les critères d’évaluation de l’étude ne savaient pas si HZ/su ou un placebo avait été administré.”
La personne qui injectait et le participant étaient donc au courant du groupe auquel le sujet était affecté (vacciné ou placebo). C’est une étude « observer-blinded ». Et le protocole a aussi été modifié sur ce point au cours de l’essai.
On peut donc avoir des doutes sur l’évaluation des « cas » de zona des participants à l’essai. Le biais est évident puisque les patients savent s’ils ont reçu le vaccin ou pas.
Chaque sujet est suivi pendant au moins 30 mois ; l’étude est terminée lorsque le nombre de cas de zona et de douleurs post-zostériennes prévus est atteint et lorsque 75% des sujets ont été suivis pendant au moins 36 mois.
L’incidence du zona est de 10 à 12,5 cas pour 1000/an chez les plus de 70 ans [9], compatible avec l’incidence de 9,2 dans le groupe placebo.
L’efficacité annoncée contre le zona est de 87,7% en réduction du risque relatif et de 2,39% en réduction du risque absolu. Elle est calculée sur une durée de 4 ans après la vaccination. On ne sait pas ce qui se passe après !
Il faut maintenant examiner en détails les effets indésirables rapportés par les auteurs.
Sécurité du vaccin
1 décès est attribué au vaccin dans l’essai clinique.
Il y a eu 29 décès dans le groupe placebo contre 17 dans le groupe vacciné (les 2 groupes sont de la même taille). Parmi des 17 décès vaccinés, 13 sont des morts subites (donc non expliquées et représentent 76% des décès enregistrés). Seules 4 morts subites sont retrouvées chez les placebo (14%).
La question se pose immédiatement de comprendre pourquoi dans 76% des décès du groupe vacciné, les médecins n’ont pas été capables de déterminer la cause de la mort alors que cela ne représente que 14% dans le groupe placebo.
Le déséquilibre des décès laisse penser que le groupe placebo était plus fragile que le groupe vacciné, Les morts subites excédentaires dans le groupe vacciné posent question, même si ce n’est sans doute pas statistiquement significatif.
Autre déséquilibre marquant, celui des cancers du poumons. Le déséquilibre en défaveur du vaccin pose également question : 18 cancers du poumon chez les vaccinés contre 10 chez les placebo (tableau S7). Mais les résultats sont incohérents car ne correspondent pas au tableau S5 ou on trouve 22 vaccinés et 13 placebo.
Parmi les effets indésirables graves, on note d’autres déséquilibres :
- 26 sepsis (infection grave) chez les vaccinés et 17 chez les placebo.
- Infection à staphylocoque: 4 vaccinés et 1 placebo.
- Les ostéoarthrites : 26 sont signalées chez les vaccinés contre 17 chez les placebo, est-ce à rapprocher des fractures par compression de la colonne vertébrale (6 vaccinés et 1 placebo) ?
Tous ces déséquilibres posent beaucoup de questions.
Finalement, la liste des effets indésirables graves reconnus en lien avec le vaccin :
- 1 infarctus du myocarde
- 1 colite
- 1 pancréatite
- 1 granulomatose éosinophilique avec polyangéite
- 4 infections (dont 1 otite herpétique)
- 1 leucémie aigüe
- 1 Guillain-Barré
- 1 eczéma
- 4 désordres généraux
- 1 lymphadénite
- 1 colite
- 1 pancréatite
Selon le rapport de 2018 de l’EMA [10], dans les essais cliniques, un décès a été attribué au vaccin.
Dans le même rapport, un autre effet indésirable grave est signalé : il s’agit d’une maladie auto-immune, le purpura thrombocytopénique (le suivi des maladies auto-immunes a été ajouté par un amendement au protocole de l’essai en 2014 ; l’essai se terminant en 2014).
L’EMA n’a donc pas tenu compte des autres effets indésirables graves reconnus en lien avec le vaccin dans l’essai de 2016. Les raisons de ces choix discutables ne sont pas connus.
D’autres effets indésirables non détectés dans les essais cliniques ont été recensés après la commercialisation du vaccin. Le Shingrix est capable, par exemple, de provoquer également un lupus. [2]
Autres problèmes concernant le Shingrix
D’autres problèmes s’ajoutent, notamment au niveau de la composition du vaccin. Le vaccin est préparé sur des cellules d’ovaires de hamster chinois et peut donc contenir des fragments d’ADN de hamster. De plus, il est adjuvanté avec l’AS01B, connu pour sa toxicité. Et pour finir, il contient du PEG 80 qui peut faciliter l’entrée dans les cellules des fragments d’ADN résiduels.
Conclusion
Quel est l’intérêt de vacciner contre une maladie que l’on a déjà contractée alors que l’immunité naturelle acquise par la maladie est définitive comme le confirme Santé Publique France [5] ?
En effet, plus de 90% des adolescents et 98% des femmes enceintes sont immunisés naturellement contre le virus de la varicelle zona en France [6]
En France, il est pourtant recommandé de vacciner uniquement les adolescents ou jeunes adultes qui n’ont pas eu la varicelle dans l’enfance.[7]
Et contrairement à ce qu’affirme le Figaro [3], le vaccin n’est pas destiné aux personnes immunodéprimées (voir l’avis de la HAS [4])
En conclusion, pourquoi les autorités françaises recommandent-elles, contradictoirement, de ne vacciner que les adolescents qui n’auraient pas eu la varicelle dans l’enfance et de vacciner tous les plus de 65 ans (qui l’ont certainement eue)?
Ce vaccin n’est pas sans danger et la démonstration de son efficacité peut être mise en doute!
[0] https://lequotidiendupharmacien.fr/exercice-pro/shingrix-victime-de-son-succes
[1] https://pubmed.ncbi.nlm.nih.gov/27626517/
[2] https://pubmed.ncbi.nlm.nih.gov/40500571/
[6] https://vaccination-info-service.fr/Les-maladies-et-leurs-vaccins/Varicelle
[7] https://vaccination-info-service.fr/Les-maladies-et-leurs-vaccins/Varicelle
[8] https://www.nejm.org/doi/suppl/10.1056/NEJMoa1603800/suppl_file/nejmoa1603800_protocol.pdf
[9] https://www.mesvaccins.net/web/news/4961-la-vaccination-contre-le-zona-recommandee-de-65-a-79-ans)
[10] https://www.ema.europa.eu/en/documents/overview/shingrix-epar-medicine-overview_pl.pdf







