Auteur(s) : Equipe des Scientifiques Indépendants
Temps de lecture : 10 minutes
À Retenir
- Aucun vaccin anti-Covid n’a permis jusqu’à maintenant d’empêcher l’infection par le SARS-CoV-2.
- Chaque variant émergeant du SARS-CoV-2 échappe à notre surveillance immunitaire
- Les derniers sous-variants Omicron sont hautement résistants in vitro à la neutralisation par les anticorps induits aussi bien par la vaccination avec les derniers boosters anti-Omicron que par une infection naturelle antérieure.
Introduction
-La circulation du SARS-CoV-2 n’est pas finie, notamment en raison de l’émergence de variants Omicron et de leurs sous-variants. Ainsi, si le sous-variant BA.5 est globalement dominant actuellement, d’autres sous-variants sont en émergence pour prendre le dessus dans ce que l’on pourrait qualifier de « soupe de variants ».
C’est ainsi que les scénarios alarmistes préviennent que de nouvelles vagues d’infections sont à venir avec BQ.1 et son descendant BQ.1.1 qui se sont largement répandus en Amérique de Nord et en Europe après avoir été détectés initialement au Nigéria au début juillet 2022. A la fin de l’automne ces variants représentaient plus de 60% des détection de SARS-CoV-2 en France. Mais en parallèle, les variants XBB et XBB.1 sont devenus prédominants dans l’Est asiatique après avoir été identifiés en Inde à la mi-août. On pense que BQ.1 et BQ1.1 ont évolué à partir de BA.5, tandis que XBB et XBB.1 proviennent de la recombinaison entre 2 sous lignages de BA.2.
D’ailleurs l’évolution de ces sous-lignages ne cessent pas, étant accompagnée d’une complexité galopante de mutations. Ainsi, la protéine Spike du variant dominant BQ.1 possède les mutations K444T et N460K en plus des mutations déjà présentes dans BA.5. Aussi, la Spike du variant prédominant XBB possède 14 mutations de plus que celles déjà dans BA.2. Finalement, on est à nouveau dans la situation subie lors de l’apparition du premier variant Omicron il y a un an, avec la même question qu’alors : est-ce que l’efficacité neutralisante de l’arsenal industriel à notre disposition (anticorps monoclonaux, préparations vaccinales) sera suffisante ?
C’est cette question à laquelle des investigateurs américains de la prestigieuse université Columbia ont tenté de répondre et pour laquelle ils ont publié un article dans la grande revue de référence en biologie moléculaire et cellulaire, Cell (en ligne depuis le 14 décembre 2022) [1].
Une neutralisation déficiente des anticorps induits par la vaccination
Pour savoir si les sous-variants d’Omicron BQ.1, BQ.1.1, XBB et XBB.1 présentaient une résistance aux anticorps produits par les populations vaccinées contre la Covid, 5 cohortes cliniques ont été examinées.
Tout d’abord 15 sérums provenaient de sujets (hommes et femmes) entre 26 et 68 ans, 14 à 90 jours après la troisième injection, en majorité de la préparation originale contre la souche Wuhan, BNT162b2 (Pfizer) ou dans 3 cas du mRNA-1273 (Moderna).
Ensuite, 19 sérums provenaient d’hommes ou de femmes entre 48 et 63 ans, 20 à 36 jours après la quatrième injection de la préparation vaccinale originale (quasi-exclusivement du Pfizer, 18 cas/19).
Le troisième groupe de 21 sérums provenaient d’hommes et de femmes (23 à 49 ans) ayant reçu 3 injections de la préparation originale puis une quatrième injection bivalente (Pfizer ou Moderna) incorporant à la fois la version Wuhan et la version BA.5 de l’ARNm codant pour la Spike. Ces sérums ont été prélevés 23 à 30 jours après la 4e injection.
Enfin, les deux derniers groupes étaient constitués de sérums de 14 et 20 sujets (entre 22 et 61 ans) ayant reçu 2, 3 ou 4 injections de la préparation originale puis ayant été infectés par les variants BA.2 ou BA.5 respectivement. Et encore une fois, les sérums ont été collectés entre 14 et 164 jours après déclaration d’infection (mais la plupart sont dans le mois qui suit).
Les chercheurs ont produit des pseudovirus correspondant aux variants avec la mutation D614G (dominant en Europe en janvier 2021, appelé aussi variant Alpha), BA.2, BA.5, BQ.1, BQ.1.1, XBB, et XBB.1. Et des cultures de cellules ont été infectées par ces pseudovirus en présence de dilutions des sérums des 5 cohortes mentionnées précédemment. La neutralisation des virus a été dosée de façon très sensible.
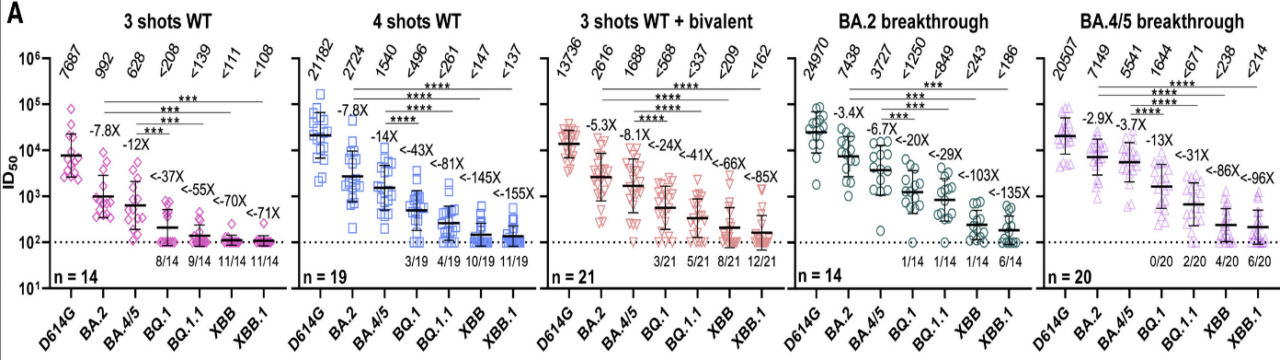
Comme attendu, toutes les souches postérieures au variant Alpha échappent mieux à leur neutralisation (sur la Figure ci-dessus, vous voyez une baisse très nette de l’ID50, pour tous les groupes, à droite de D614G et l’amplitude de la diminution est indiquée au-dessus des points de mesure). Mais de façon alarmante, la réduction de la neutralisation atteint des facteurs supérieurs à 70 fois avec les variants plus récents chez des sujets triplement injectés.
Par ailleurs, bien que quasiment tous les sérums présentent des anticorps contre les variants BA.2 et BA.5, une majorité de sérums, en condition de plus faible dilution, ne parviennent pas à neutraliser le virus. Cette tendance est observée dans les autres cohortes et c’est le variant XBB.1 qui échappe le plus à la neutralisation, suivi de XBB, BQ.1.1 et BQ.1.
On note également que le pouvoir de neutralisation est sensiblement meilleur avec les sérums de sujets infectés par BA.2 ou BA.5 qu’avec 4 injections ou 3 injections originales et le bivalent. Ce qui pourrait laisser penser que la rencontre du virus entier vivant est plus immunogène que la vaccination à ARNm telle que proposée actuellement.
Les résultats des tests de neutralisation ont permis aux auteurs de construire une carte antigénique pour décrire l’éloignement relatif entre les différents variants testés. Ils anticipent ainsi que le variant XBB.1, dans sa dérive antigénique, s’est déjà autant éloigné de BA.5 que celui-ci ne s’était éloigné d’Alpha. Ainsi XBB.1 serait environ 63 fois plus résistant à la neutralisation par les anticorps sériques que BA.2 et 49 fois plus résistant que BA.5.
Des anticorps monoclonaux sans réponse
Pour comprendre d’où vient la perte d’activité neutralisante des anticorps sériques contre les variants BQ.1, BQ.1.1, XBB et XBB.1, Wang et ses collaborateurs ont testé un panel de 23 anticorps monoclonaux qui ciblent différents motifs tridimensionnels (épitopes) de la protéine Spike.
Il est important de noter que tous ces anticorps monoclonaux ont à l’origine une activité appréciable contre le premier variant Omicron, et d’ailleurs 4 sont destinés à la clinique : tixagevimab, cilgavimab (les 2 formant Evusheld), bebtelovimab, et sotrovimab.
C’est ainsi que des anticorps autorisés en clinique sont tout simplement inactifs contre BQ.1 et BQ.1.1. Dans le détail, 19 des 23 anticorps monoclonaux testés ont perdu majoritairement ou complètement leur activité de neutralisation contre XBB et XBB.1. Et même parmi ceux qui restent, 3 ont déjà perdu une partie de leur activité contre BA.2 quand on la compare à celle contre le variant Alpha. Ainsi plusieurs mutations de la Spike sont pointées du doigt et des modélisations structurales permettent d’expliquer les pertes d’activité des anticorps monoclonaux.
Une cible de Spike toujours aussi bien atteinte par les nouveaux variants
L’enzyme de conversion de l’angiotensine 2 (ACE2) est la porte d’entrée du virus SARS-CoV-2 dans les cellules et le degré d’affinité que présente Spike pour ce récepteur peut influencer la transmissibilité du virus.
Les chercheurs ont généré in vitro des protéines Spike, avec les mutations adéquates pour qu’elles correspondent à ce que produit chacun des 4 variants étudiés (BA.5, BQ.1, BQ.1.1, XBB et XBB.1). Ils ont ensuite mesuré la force de la liaison transitoire qui peut s’établir entre la version humaine d’ACE2 et les différentes formes de protéine Spike.
Il semble que BQ.1 et BQ.1.1 aiment ACE2 tout autant que BA.5. On note une légère baisse d’affinité de XBB et XBB.1 comparativement à BA.2. Mais finalement ce qui importe le plus, c’est qu’il semble exclu que l’émergence des nouveaux sous-variant d’Omicron soit due à une plus grande affinité pour ACE2.
Limitations de l’étude
D’une part, les résultats obtenus sont le fruit de manipulations in vitro, qui même si elles semblent en général prédictives de la situation observée in vivo ne peuvent remplacer la réalité clinique qu’il faudra observer attentivement dans les mois à venir.
D’autre part, la principale limite de l’étude est liée à l’absence de test de l’immunité cellulaire face aux nouveaux sous-variants d’Omicron. N’oublions pas que les premières barrières contre le SARS-CoV-2 incluent des cellules de l’immunité innée et que consécutivement aux injections vaccinales une éducation de lymphocytes T doit permettre une action coordonnée avec celle des cellules qui produisent des anticorps dirigés contre la protéine Spike.
Notre capacité à cohabiter avec le SARS-Cov-2 dépend des différents bras armés de notre immunité innée et adaptative et il serait trop hâtif de limiter l’efficacité ou l’échec complet des stratégies vaccinales en ne se basant que sur la production d’anticorps neutralisant.
Conclusions
Comme un oiseau de mauvais augure, cette étude annonce que les nouveaux sous-variants émergeants d’Omicron vont être capables d’infecter les gens vaccinés comme s’ils ne l’étaient pas.
Pourtant, ce n’est pas nouveau, d’autres variants ont précédemment mis KO des anticorps thérapeutiques (bamlanivimab, etesevimab, imdevimab, casirivimab, tixagevimab, cilgavimab, et sotrovimab).
C’est très ennuyeux car si l’on s’en tient aux résultats présentés, on n’a en fait rien d’efficace pour les millions de sujets immunodéprimés pour lesquels les vaccins COVID-19 ne sont pas adaptés [2].
Par ailleurs, comme une ritournelle, à chaque nouvelle préparation vaccinale, une publication dans un journal de référence pour claironner que « ça marche » ! Dernière étude en date du 15 novembre 2022 des gourous de BioNTech, Ugur Sahin et Özlem Türeci dans Science Immunology. Ils nous expliquent que les préparations vaccinales bivalentes contre les sous-variants d’Omicron BA.4/BA.5 nous permettent de produire des anticorps neutralisants redoutablement efficaces [3].
Dommage donc que ce soit déjà trop tard…Il serait peut-être temps d’arrêter de laisser tourner la platine avec une disque rayé et de penser à changer de stratégie…
Références
[1] https://www.sciencedirect.com/science/article/pii/S0092867422015318
[2] https://reinfocovid.fr/science/1-2-3-4-5-doses-et-toujours-rien-chez-des-immunodeprimes-explication/
[3] Muik A, Lui BG, Bacher M, Wallisch AK, Toker A, Couto CIC, Güler A, Mampilli V, Schmitt GJ, Mottl J, Ziegenhals T, Fesser S, Reinholz J, Wernig F, Schraut KG, Hefesha H, Cai H, Yang Q, Walzer KC, Grosser J, Strauss S, Finlayson A, Krüger K, Ozhelvaci O, Grikscheit K, Kohmer N, Ciesek S, Swanson KA, Vogel AB, Türeci Ö, Sahin U. Exposure to BA.4/5 S protein drives neutralization of Omicron BA.1, BA.2, BA.2.12.1, and BA.4/5 in vaccine-experienced humans and mice. Sci Immunol. 2022 Dec 23;7(78):eade9888. doi: 10.1126/sciimmunol.ade9888. Epub 2022 Dec 23. PMID: 36378074; PMCID: PMC9765452. (article disponible gratuitement en ligne : https://pubmed.ncbi.nlm.nih.gov/36378074/)